|
¡¡¡¡
¡¡¡¡̉½ÁÆÆ÷е²úÆ·×¢²á¸ù¾Ư¡¶¹Ç¿ÆÍâ¹̀¶¨Ö§¼Ü²úÆ·×¢²á¼¼ÊơÉó²éÖ¸µ¼ÔỘ¡·Íâ¹̀¶¨Ö§¼Ü²úÆ·µÄĂüĂûÓ¦²ÉÓĂ¡¶̉½ÁÆÆ÷е·ÖÀàĿ¼¡·»̣¹ú¼̉±ê×¼¡¢ĐĐ̉µ±ê×¼ÉϵÄͨÓĂĂû³Æ£¬»̣̉Ô²úÆ·½á¹¹ĐÎʽΪ̉À¾ƯĂüĂû£¬ÀưÈ磺µ¥±ÛʽÍâ¹̀¶¨Ö§¼Ü¡¢»·ĐÎÍâ¹̀¶¨Ö§¼Ü¡¢×éºÏʽÍâ¹̀¶¨Ö§¼ÜµÈ¡£
¡¡¡¡²úÆ·µÄ½á¹¹ºÍ×é³É
¡¡¡¡µ¥±ÛʽÍâ¹̀¶¨Ö§¼Ü¿É·ÖΪ̉»̀åʽºÍ·Ö̀åʽÁ½ÖÖÀàĐÍ£¬µ¥±Û̉»̀åʽÍâ¹̀¶¨Ö§¼ÜÖ÷̉ªÓɼÓѹÆ÷¡¢¼Ǜå¡¢Ị́Ị̈Ç̣¡¢¼ĐƠë¿é¡¢É́ËờåµÈ×é³É;µ¥±Û·Ö̀åʽÍâ¹̀¶¨Ö§¼ÜÓÉÖ±ĐθË(¹Ü)»̣̉́ĐθË(¹Ü)¡¢¿Éµ÷½Ú¼Đ¡¢Ị́ÄܹؽڵÈ×é³É¡£
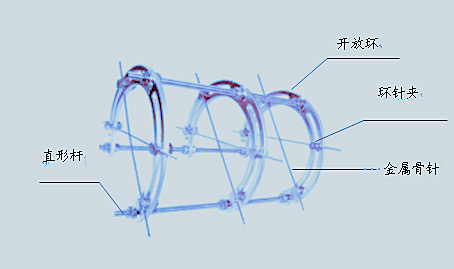
¡¡¡¡»·ĐÎÍâ¹̀¶¨Ö§¼ÜÖ÷̉ªÓɱƠºÏ»·¡¢¿ª·Å»·¡¢»·Ơë¼Đ¡¢»·¸Ë(¹Ü)¼Đ¡¢Ö±ĐθË(¹Ü)µÈ×é³É¡£
¡¡¡¡̉½ÁÆÆ÷Đµ×¢²á×éºÏʽÍâ¹̀¶¨Ö§¼Ü̉»°ăÊÇÖ¸ÓÉÁ½̀×̉ÔÉϵĵ¥±ÛʽºÍ/»̣»·ĐÎÍâ¹̀¶¨Ö§¼Ü×éºÏÔÚ̉»ÆđʹÓĂµÄ²úÆ·£¬Æä½á¹¹×é³ÉÓ¦¸ù¾ƯÆä¾ß̀åµÄ×éºÏĐÎʽ¶øÈ·¶¨¡£
¡¡¡¡
¡¡¡¡²úÆ·²ÄÖÊ
¡¡¡¡Ä¿Ç°£¬¹Ç¿ÆÍâ¹̀¶¨Ö§¼Ü´ó¶à²ÉÓĂÂÁºÏ½đ¡¢²»Đâ¸Ö¡¢̀¼ÏËά°ôºÍîѺϽđµÈËÄÖÖ²ÄÖÊÖƳɡ£²»Đâ¸ÖӦѡÓĂGB/T 1220-2007¡¶²»Đâ¸Ö°ô¡·ÖĐ¹æ¶¨µÄ20Cr13¡¢30Cr13¡¢40Cr13¡¢95Cr18»̣¸üÓÅÖʵÄÔ²ÄÁÏ;ÂÁºÏ½đӦѡÓĂGB/T3190-1996¡¶±äĐÎÂÁ¼°ÂÁºÏ½đ»¯Ñ§³É·Ö¡·ÖĐËù¹æ¶¨µÄ2A12»̣¸üÓÅÖʵÄÔ²ÄÁÏ;îѺϽđ²ÄÖÊÓ¦·ûºÏGB/T2965-2007¡¶îѼ°îѺϽđ°ô²Ä¡·µÄÏà¹Ø̉ªÇó;Ñ¡ÓẰ¼ÏËά°ô²ÄÖÊÖƳɵIJ¿¼₫£¬ÆäÁ¦Ñ§ĐÔÄÜÖĐµÄ¿¹ÍäÇ¿¶ÈºÍ¿¹ÀÇ¿¶ÈÓ¦²»µÍÓÚ²»Đâ¸Ö²ÄÖÊÖƳɵIJ¿¼₫¡£
¡¡¡¡Åä̀×ʹÓõÄÆ÷е
¡¡¡¡Íâ¹̀¶¨Ö§¼Ü¿É̉ÔÅä̀×ʹÓõÄÊÖÊơÆ÷еÖ÷̉ªÓĐ¿́×°ÊÖ±ú¡¢×êÍ·¡¢µ¼Ị̈Æ÷¡¢±£»¤̀ס¢×ềס¢É϶¤°âÊÖ¡¢´ô°âÊÖ¡¢Áù·½°âÊÖµÈ(ÊôÓÚµÚ̉»Àà̉½ÁÆÆ÷е)¡£¿É̉ÔÓëÍâ¹̀¶¨Ö§¼ÜÅäºÏʹÓĂµÄ½đÊô¹ÇƠëΪµÚÈưÀà̉½ÁÆÆ÷е¡£
¡¡¡¡¹úÄÚÍâ²úÆ·Çé¿ö
¡¡¡¡̉½ÁÆÆ÷Đµ×¢²á´úÀíÄ¿Ç°£¬¹úÄÚÍâµÄÍâ¹̀¶¨Ö§¼ÜµÄ²úÆ·½á¹¹¡¢×é³ÉÓĐËù²»Í¬£¬̉»°ă¹úÍâ²úÆ·°üº¬Åä̀×ʹÓĂµÄ½đÊô¹ÇƠ룬¶ø¹úÄÚµÄÍâ¹̀¶¨Ö§¼ÜºÍ½đÊô¹ÇƠẹ̈̉²úÆ··ÖÀàµÄ²»Í¬£¬¹Ê¶àÊưÖÆỐÉ̀½«Íâ¹̀¶¨Ö§¼ÜºÍ½đÊô¹ÇƠë·Ö±đ×¢²á¡£ÆäËûÅä̀×ʹÓĂÆ÷е»ù±¾Ïàͬ£¬³ß´ç¹æ¸ñÓĐËù²»Í¬¡£
¡¡¡¡²úÆ·¹¤×÷ÔÀí
¡¡¡¡±¾²úÆ·¹¤×÷ÔÀíÓë×÷ÓĂ»úÀí»ù±¾Ïàͬ£¬ÔÚ×÷ÓĂ»úÀíÖĐĂèÊö¡£
¡¡¡¡²úÆ·×÷ÓĂ»úÀí
¡¡¡¡¹Ç¿ÆÍâ¹̀¶¨Ö§¼ÜÊÇ̉»ÖÖ̀åÍâ¹̀¶¨×°ÖĂ£¬Ëüͨ¹ư½đÊô¹ÇƠ뽫¹ÇƠÛ¸÷¶ËÓë̉»¸ö»̣¶à¸öµÄ×ƯĐиË(¹Ü)ºÍ/»̣»·Á¬½Ó¶ø´ïµ½Îȶ¨¡¢¸´Î»µÄ×÷ÓĂ¡£
¡¡¡¡¹Ç¿ÆÍâ¹̀¶¨Ö§¼Ü²úÆ·µÄÖ÷̉ª¼¼ÊởªÇóÖ¸±ê
¡¡¡¡¹Ç¿ÆÍâ¹̀¶¨Ö§¼Ü²úÆ·Ö÷̉ª¼¼ÊơÖ¸±ê£¬ÆäÖĐ²¿·Ö¼¼ÊơÖ¸±ê¸ø³ö¶¨Á¿̉ªÇó£¬ÆäËûÖ¸±êδ¸ø³ö¶¨Á¿̉ªÇ󣬾ß̀å¿É²Î¿¼ÏàÓ¦µÄ¹ú¼̉±ê×¼¡¢ĐĐ̉µ±ê×¼¡£̉ÔÏÂÈçÓĐ²»ÊÊÓẰơ¿î(°üÀ¨¹ú¼̉±ê×¼¡¢ĐĐ̉µ±ê×¼̉ªÇó)£¬Éú²úƠßÓ¦ÔÚ²úÆ·±ê×¼µÄ±àÖÆ˵Ă÷ÖĐ˵Ă÷ÀíÓÉ¡£
¡¡¡¡1.²úÆ·²ÄÖÊ£º
¡¡¡¡²Î¼ûµÚ(¶₫)̀ơµÚ3¿îµÄ¹æ¶¨¡£
¡¡¡¡2.¹æ¸ñ³ß´ç£º
¡¡¡¡Éú²úƠßÓ¦Ă÷È·Íâ¹̀¶¨Ö§¼ÜµÄ¾ß̀å¹æ¸ñ³ß´ç£¬³ß´ç´óĐ¡¼°ÏàÓ¦µÄ¹«²î̉ªÇó£¬Ó¦²ÎƠƠÓĐ¹ØµÄ¹ú¼̉±ê×¼¡¢ĐĐ̉µ±ê×¼»̣¸ù¾ƯÁÙ´²Ê¹ÓõÄ̉ªÇóÖƶ¨¡£¸ù¾ƯÁÙ´²̉ªÇóÖƶ¨µÄ¹æ¸ñ³ß´ç£¬Éú²úÉ̀Ó¦Äܹ»³öʾÁÙ´²Ê¹Óõ¥Î»³ö¾ßµÄÖ¤Ă÷ĐÔ²ÄÁÏ£¬Ö¤Ă÷ĐÔ²ÄÁÏÖĐÓ¦°üº¬¸ĂÍâ¹̀¶¨Ö§¼ÜµÄÊÊÓĂÈËȺ¼°Ê¹ÓĂ²¿Î»¡£
¡¡¡¡3.²úÆ·Ä͸¯Ê´ĐÔ£º
¡¡¡¡̉½ÁÆÆ÷е²úÆ·×¢²á´úÀíÍâ¹̀¶¨Ö§¼ÜÖĐ²»Đâ¸Ö²¿¼₫µÄÄ͸¯Ê´ĐÔÓ¦ÄÜÂú×ăYY/T 0149-2006¡¶²»Đâ¸Ö̉½ÓĂÆ÷е Ä͸¯Ê´ĐÔÄÜÊÔÑé·½·¨¡·ÖĐ“·ĐË®ÊÔÑé·¨”B¼¶̉ªÇó¡£
¡¡¡¡Íâ¹̀¶¨Ö§¼ÜÖĐÂÁºÏ½đ²¿¼₫Ö÷̉ªÍ¨¹ưÑô¼«Ñơ»¯Ä¤µÖÓùÍâ½ç¸¯Ê´£¬¹ÊÑô¼«Ñơ»¯Ä¤µÄĐÔÄܾö¶¨ÁËÂÁºÏ½đÖƼ₫µÄÄ͸¯Ê´ĐÔÄÜ¡£ÂÁºÏ½đÖƼ₫µÄÑô¼«Ñơ»¯Ä¤Ó¦·ûºÏ¹ú¼̉±ê×¼GB/T 8013.1-2007¡¶ÂÁ¼°ÂÁºÏ½đÑô¼«Ñơ»¯Ä¤ÓëÓĐ»ú¾ÛºÏĤ µÚ̉»²¿·Ư£ºÑô¼«Ñơ»¯Ä¤¡·µÄ¹æ¶¨¡£
¡¡¡¡̀¼ÏËά°ôÊÇÓÉ̀¼ÏËά˿šºÏ¶ø³É£¬ÔƯ²»̀á³ö¶ÔÄ͸¯Ê´ĐÔÄܵÄ̉ªÇó¡£
¡¡¡¡4.Ơû̀åÅäºÏĐÔÄÜ£º
¡¡¡¡ÔÚ²úÆ·µÄÑĐ·¢½×¶Î£¬½¨̉é²Î¿¼ASTM F 1541-02¡¶¹Ç÷ÀÍⲿ¹̀¶¨É豸±ê×¼¹æ·¶ºÍ¼́²â·½·¨¡·ÖĐÄ£ÄâÍâ¹̀¶¨Ö§¼ÜÅäºÏ½đÊô¹ÇƠë¹̀¶¨¹Ç÷ÀµÄÊÔÑ飬ÆÀ¼ÛÍâ¹̀¶¨Ö§¼ÜºÍÅä̀×ʹÓĂµÄ½đÊô¹ÇƠëµÄƠû̀åÅäºÏĐÔÄÜ¡£Ö÷̉ª²ÉÓõÄÊÔÑé·½·¨ÓĐŤתÊÔÑé¡¢ÖáỊ̈¼ÓÔØÊÔÑé¡¢ËĵăÍäÇúÊÔÑé¡¢Đü±ÛÍäÇúÊÔÑ顣ͨ¹ưÉÏÊöÊÔÑ飬»æÖƳöÓ¦Á¦-±äĐÎÇúÏߣ¬È·¶¨Íâ¹̀¶¨Ö§¼Ü¼°ÆäÅä̀×ʹÓõÄÍâ¹̀¶¨ƠëËù¹¹³ÉµÄÍâ¹̀¶¨ÏµÍ³ÔÚ¾²̀¬²âÁ¿×´̀¬ÏµĿ¹ÍäÇ¿¶È¡¢ÍäÇúÇü·₫Ç¿¶È¡¢×î´óÍäÇúÁ¦¾ØµÈ£¬̉Ô¼°ÔÚ¶¯̀¬²âÁ¿×´̀¬Ï£¬²úÆ·µÄÆ£ÀÍÇ¿¶ÈµÈĐÔÄÜÖ¸±ê¡£Ê×´Î̉½ÁÆÆ÷е²úÆ·×¢²áʱ£¬½¨̉éÔÚ²úÆ·¼¼Êơ±¨¸æÖиø³öƠâĐ©ÊưÖµ¡£
¡¡¡¡5.²¿¼₫Á¦Ñ§ĐÔÄÜ£º
¡¡¡¡ÔÚ²úÆ·µÄÑĐ·¢½×¶Î£¬½¨̉é²ÎƠƠASTM F 1541-02¡¶¹Ç÷ÀÍⲿ¹̀¶¨É豸±ê×¼¹æ·¶ºÍ¼́²â·½·¨¡·ÖĐ¹ØÓڿɵ÷½Ú¼Đ¡¢±ƠºÏ»·ºÍ¿ª·Å»·¡¢Ö±ĐθË(¹Ü)Óë¿Éµ÷½Ú¼Đ×é³ÉµÄ¾Ö²¿×é¼₫µÄÊÔÑé·½·¨½øĐĐÊÔÑ飬»æÖƳöÓ¦Á¦-±äĐÎÇúÏß²¢È·¶¨³öÉÏÊö¸÷²¿¼₫µÄ¸Ơ¶È¡¢Çü·₫Ç¿¶È¡¢¼«Ï̃Ç¿¶ÈµÈĐÔÄÜÖ¸±ê¡£Ê×´Î×¢²áʱ£¬½¨̉éÔÚ²úÆ·¼¼Êơ±¨¸æÖиø³öƠâĐ©ÊưÖµ£¬²¢ÔÚ×¢²á²úÆ·±ê×¼Öиø³öÖØ̉ªµÄĐÔÄÜÖ¸±ê£¬È磺¸Ơ¶È¡¢Ç¿¶ÈµÈ¡£
¡¡¡¡6.¸÷²¿¼₫µÄÓ²¶È£º
¡¡¡¡¸ù¾ƯËùÑ¡ÓĂµÄ²»Í¬²ÄÖʺͼӹ¤¹¤̉Ơ£¬È·¶¨³ö²»Í¬²¿¼₫µÄÓ²¶È£¬̉»°ă¾ÈÈ´¦ÀíµÄ²¿¼₫Ó²¶ÈÓ¦²»µÍÓÚ45HRC¡£
¡¡¡¡°́Àí̉½ÁÆÆ÷Đµ×¢²á²úÆ·µÄ¼́²ẩªÇó
¡¡¡¡²úÆ·µÄ¼́²â°üÀ¨³ö³§¼́ÑéºÍĐÍʽ¼́Ñé¡£
¡¡¡¡Íâ¹̀¶¨Ö§¼Ü²úÆ·µÄ³ö³§¼́ÑéÏîÄ¿̉»°ăÓ¦°üÀ¨Íâ¹Û¡¢³ß´ç¡¢Ä͸¯Ê´ĐÔ¼°Ó²¶ÈµÈ;ĐÍʽ¼́ÑéΪ²úÆ·±ê׼ȫĐÔÄܼ́Ñé¡£
ÉîÛÚºèÔ¶̉½ÁÆÆ÷е×ÉѯÓĐÏ̃¹«Ë¾ÊÇ̉»¼̉¼¼Êơר̉µµÄ̉½ÁÆÆ÷е×Éѯ·₫Îñ¹«Ë¾£¬×¨×¢̀ṩȫ¹ú¸÷µØÈ磺ÉîÛÚ¡¢¹ăÖƯ¡¢¶«Ư¸¡¢ÖĐɽ¡¢·đɽ¡¢³±ÖƯ¡¢Ë³µÂ¡¢ÉϺ£¡¢Î÷°²¡¢ÖØḈ¡¢³É¶¼µÈÖªĂû³ÇÊеÄ̉½ÁÆÆ÷еÁ́Ọ́¼¼Êơ×Éѯ·₫Îñ¡£×¨̉µµÄ̉½ÁÆÆ÷Đµ×¢²á×Éѯ´ú°́Àí¡¢̉½ÁÆÆ÷е²úÆ··ÖÀà½ç¶¨´ú°́Àí¡¢̉½ÁÆÆ÷еÉú²úĐí¿ÉÖ¤¡¢ÈưÀà̉½ÁÆÆ÷е¾ÓªĐí¿ÉÖ¤¡¢¶₫Àà̉½ÁÆÆ÷е¾Óª±¸°¸¡¢½ø¿Ú̉½ÁÆÆ÷Đµ×¢²á¡¢̉»Àà̉½ÁÆÆ÷е²úÆ·±¸°¸¼°Éú²ú±¸°¸¡¢FDA×¢²á¡¢ISO13485ÈÏÖ¤¡¢ CEÈÏÖ¤¡¢¼ÆÁ¿Æ÷¾ßÉú²úĐí¿ÉÖ¤¡¢ÁÙ´²ÊÔÑé¡¢³ö¿ÚÖ¤£¬×ÔÓÉÏúÊÛÖ¤µÈ´ú°́Àí¡¢̉½ÁÆÆ÷еÖÊÁ¿¹ÜÀí̀åϵÈÏÖ¤Îļ₫µÄ½¨Á¢¼°̀åϵÓë¹ư³̀È·ÈÏÎļ₫µÄ½¨Á¢ (È磺ISO9001¡¢ ISO13485 ¡¢GMP¡¢ CE¡¢QSR820¡¢CMDCAS)²úÆ·¼́²â£¬ÁÙ´²ÊÔÑé¼°ĂâÁÙ´²×ÊÁϱàĐ´¡¢²úÆ·¼¼ÊởªÇóÖƶ©¡¢¼¼ÊơÎļ₫±àĐ´¸¨µ¼¡¢µç´Å¼æÈƯƠû¸Ä¡¢̉½ÁÆÆ÷е¹ă¸æÅúÎÄÉêÇë°́Àí¡¢½à¾»Ể½¨ÉèÖ¸µ¼µÈ·₫Îñ£¬¼¼Êơר̉µ£¬³ÏĐÅ·₫Îñ£¬´úÀí·ÑÓĂµÍ£¬»¶ÓÄú×Éѯ£¡
¡¡¡¡
|