|
医疗器械产品注册一次性医用喉罩技术要求怎样编写?产品的主要技术指标是个什么?
一次性医用喉罩医疗器械注册指标根据《一次性医用喉罩产品注册技术审查指导原则》,本条款给出一次性医用喉罩需要考虑的产品基本技术性能指标,企业应参考相应的国家标准、行业标准,根据企业自身产品的技术特点制定相应的医疗器械注册产品标准。以下技术指标如有不适用生产企业产品的条款(包括国家标准、行业标准要求),应该在注册标准编制说明中说明理由。
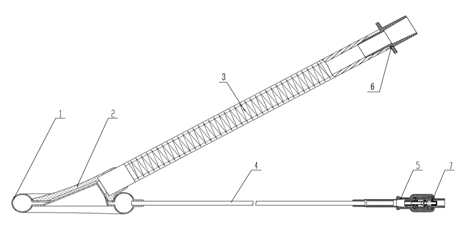
医疗器械注册一次性医用喉罩
1. 物理性能:
(1) 产品型号、规格、尺寸、外观
应由生产企业根据实际产品在医疗器械注册产品标准中具体编写。
喉罩的规格设计一般遵循以下协定:
1)规格范围应从0到6,允许的最小增量是0.5;
2)规格0到6应设计对应产品规格从最小到最大,从儿童到成人过渡的规格是3。
对加强型喉罩外观应包括支撑钢丝不得外露。
(2)通气开口
在喉罩的病人端或病人端附近要有一个允许通气的孔,可以做一个辅助通气开口以降低堵塞的风险。
(3)连接牢固度
接头与通气管、充气管与气囊、通气管与连接件连接应牢固,在承受15N轴向静拉力作用下持续15s,不得脱落或分离、断裂。
(4)接头
1)机器端应为一个15mm的外圆锥接头,尺寸应符合YY 1040.1—2003中的规定。内径的任何变化都应该是渐进的,方便器械穿过和移动。
2)病人端开口应有一个与接头病人端的长轴成90°±5°的平面。
(5)充气系统
1)充气系统应包括一根充气管、一个指示球囊或其他能够指示充气或放气的装置。
2)充气管的自由端应是开口的,用一个密封装置或充气阀封闭。如果需要与外部充气装置有接触面,充气管自由端应能够与装有符合GB/T 1962.1-2001的6%(鲁尔)外圆锥接头相匹配。
3)气囊放气时,充气管、充气阀或其他起单向阀作用的密封装置不应阻碍放气。
(6)密封性
1)在10cmH2O的正压下,最少3s内气囊密封不应产生可听的泄漏。
注:应通过临床研究测试来检验是否符合要求。功能测试器或患者模拟器不应用来验证喉罩的性能。临床研究应记录在保证声明的产品性能的条件下的测试结果。临床研究应符合ISO 14155-1和ISO 14155-2的要求。因此,该项要求可不写入医疗器械注册产品标准,但应提供临床研究测试资料。
2)喉罩气囊、通气管、充气系统及各连接处应密封良好,应无漏气现象。
(7)气囊不能堵塞通气开口或导致呼吸通路塌陷。
注:应通过对生产企业选择的、基于对风险评估和相应的验证、确认研究中风险降低措施的方法的检查来评价是否符合要求。因此,该项要求可不写入医疗器械注册产品标准,但应提供评价研究资料。
(8)生产企业应制定通气管内腔抗弯曲能力要求。
(9)生产企业应制定内腔容积的要求。
(10)生产企业应规定能够容易穿过呼吸通路的器械的最大规格(如适用)。
(11)通气管管体标识
1. 生产企业的名称或商标;
2)用粗体标记规格,包含一系列规格的喉罩应标明相应的范围;
3)“一次性使用”字样或等效标识;
4)标称插入深度标记或指示,它围绕在上喉部通气道的管身上,对应于患者的门齿或牙龈,用来指示预期插入深度的典型范围;
注:插入深度范围标记不需要在管身整个圆周上连续标记出来。
5)从通气开口病人端开始,以cm为单位标出深度标识(如提供)。
(12)标记的材料应:
1)能抵抗因麻醉剂引起的老化;
2)在使用过程中保持字迹清晰。
2. 化学性能:
医疗器械产品注册根据不同材料特性,由企业决定是否对化学性能提出要求,至少应包括pH值。用环氧乙烷灭菌的产品应规定环氧乙烷残留量的要求,应不大于10μg/g。
3. 生物性能:
一次性医用喉罩应以无菌形式提供,并进行细胞毒性、口腔粘膜刺激、迟发型超敏反应的生物学评价。
深圳鸿远医疗器械咨询有限公司专业代办医疗器械产品注册证代理咨询、医疗器械生产许可证、医疗器械经营许可证、二类医疗器械经营备案、进口医疗器械注册、一类医疗器械产品备案及生产备案、FDA注册、ISO13485认证、 CE认证、计量器具生产许可证、临床试验、出口证,自由销售证等代理代办、医疗器械质量管理体系认证文件的建立及体系与过程确认文件的建立 (如:ISO9001、 ISO13485 、GMP、 CE、QSR820、CMDCAS)产品检测,临床试验及免临床资料编写、产品技术要求制订、技术文件编写辅导、洁净室建设指导等服务,技术专业,诚信服务,代理费用低,欢迎您咨询!
|