|
2018年医疗器械临床试验备案办理条件
申办者应当在临床试验项目经伦理审查通过并与临床试验机构签订协议或合同后,填写《医疗器械临床试验备案表》,提交备案表中列出的相关材料。
2018年医疗器械临床试验备案网上办理流程
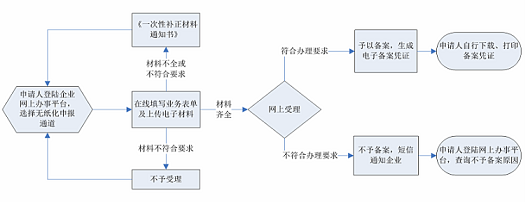
1、申请:实行无纸化申报,可登录广东省政务服务网进行网上申报工作,填报申请事项材料,证明材料以扫描件上传。所有申报资料内容必须真实、合法,文字、图案清楚;电子扫描件需加盖申请人印章,为pdf扫描件,每个文件大小不能超过10M,按照系统要求上传至办事平台。
2.资料接收:受理大厅收到申请材料后,作出资料接收或不予接收决定。申请材料不齐全或者不符合法定形式的,当场或者在5日内一次告知申请人需要补正的全部内容,逾期不告知的,自收到申请材料之日起即为受理。
3.受理:实施机关对申请资料进行形式审查。申请被受理的,申请人可获得实施机关出具的受理凭证;申请不被受理的,申请人可获得实施机关出具的不予受理通知书,不予受理通知书的内容包括不予受理的理由。
4.获取结果:申请人可登陆广东省食品药品监督管理局公众网首页审批查询栏进行办理进度查询,登陆企业申报端获取电子证书。
2018年医疗器械临床试验备案窗口办理流程
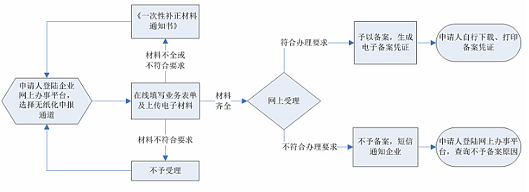
1、申请:实行无纸化申报,可登录广东省政务服务网进行网上申报工作,填报申请事项材料,证明材料以扫描件上传。所有申报资料内容必须真实、合法,文字、图案清楚;电子扫描件需加盖申请人印章,为pdf扫描件,每个文件大小不能超过10M,按照系统要求上传至办事平台。
2.资料接收:受理大厅收到申请材料后,作出资料接收或不予接收决定。申请材料不齐全或者不符合法定形式的,当场或者在5日内一次告知申请人需要补正的全部内容,逾期不告知的,自收到申请材料之日起即为受理。
3.受理:实施机关对申请资料进行形式审查。申请被受理的,申请人可获得实施机关出具的受理凭证;申请不被受理的,申请人可获得实施机关出具的不予受理通知书,不予受理通知书的内容包括不予受理的理由。
4.获取结果:申请人可登陆广东省食品药品监督管理局公众网首页审批查询栏进行办理进度查询,登陆企业申报端获取电子证书。
2018年医疗器械临床试验备案材料清单:
1、 医疗器械临床试验备案表
2、 申办者或代理人营业执照(可通过系统自动获取)
3、 伦理委员会意见
4、 申办者与临床试验机构实施临床试验协议或合同
5、 医疗器械临床试验批件(需进行临床试验审批的第三类医疗器械)
来源于:深圳鸿远医疗器械咨询有限公司 http://www.hongyuanyixiezixun.com !
|